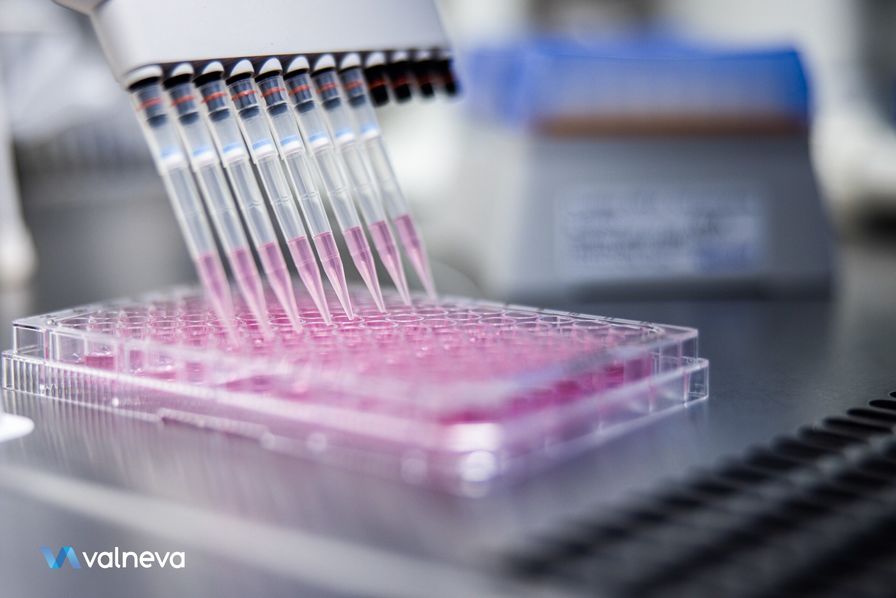
Valneva tient-elle une forme de revanche ? La biotech a connu une rentrée agitée, marquée notamment par l’abandon par le Royaume-Uni de son contrat phare qui portait sur une commande de 100 millions de doses de son vaccin.
Une annonce qui avait fait dévisser le cours en Bourse de Valneva et avait suscité de nombreuses interrogations sur l’efficacité de son candidat-vaccin contre le Covid-19, le VLA2001.
Des doutes que la biotech vient peut-être de lever avec des résultats positifs de l’essai de phase III. Réalisé sur 4 012 participants âgés de 18 ans et recrutés sur 26 sites au Royaume-Uni, cet essai avait pour objectif de comparer la réponse immunitaire suscitée par le vaccin de la biotech nantaise à celle du vaccin, déjà approuvé, du laboratoire britannique AstraZeneca.
Et cette étude a atteint ses deux critères principaux d’évaluation, puisque le VLA2001 a généré des niveaux d’anticorps supérieurs à ceux du vaccin d’AstraZeneca, ainsi qu’un taux de séroconversion des anticorps neutralisants supérieur, à 95 %, deux semaines après la deuxième injection.
Le vaccin a, en outre, entraîné une large réponse des lymphocytes T, qui contribuent à la mémoire immunitaire à long terme. Concernant les effets secondaires, l’actif affiche un profil de tolérance meilleur que celui du vaccin d’AstraZeneca.
« Ces excellents résultats confirment les avantages souvent associés aux vaccins à virus entiers inactivés », a déclaré Thomas Lingelbach, le directeur général de Valneva. Contrairement aux vaccins de Moderna et Pfizer/BioNTech, à ARNm, le vaccin de Valneva est composé de particules inactivées du virus SARS-CoV-2, avec une forte densité de protéines S (ou protéines Spike), conjuguées à deux adjuvants, l’alum et le CpG 1018.
Désormais, la biotech souhaite avancer vers une autorisation de mise sur le marché pour son vaccin. « Nous sommes déterminés à faire enregistrer notre candidat-vaccin différencié le plus rapidement possible et nous continuons de croire que nous pourrions apporter une contribution majeure à la lutte mondiale contre la pandémie de Covid-19. Nous avons hâte de proposer une solution vaccinale alternative aux personnes qui n’ont pas encore été vaccinées. »
Une concurrence féroce sur le marché
Concrètement, Valneva espère bientôt avoir le verdict de l’agence britannique du médicament, avec laquelle la biotech a démarré une évaluation en continu depuis le mois d’août 2021. La demande d’autorisation devrait ainsi être finalisée dès le mois de novembre. Valneva espère décrocher un premier feu vert à la fin de l’année 2021.
Pour l’Europe, la biotech est encore en discussion avec l’EMA, l’agence européenne du médicament, et annonce avoir déjà inclus des données issues d’une étude complémentaire portant sur l’efficacité de son vaccin chez les personnes âgées. Car Valneva compte bien pousser son avantage et poursuivre l’évaluation de son vaccin sur d’autres populations. La biotech a ainsi démarré des études portant sur l’efficacité de son vaccin en dose rappel mais aussi chez les adolescents et les personnes âgées.
En 2022, ce sont des essais sur des populations pédiatriques et des études de phase III en rappel qui devraient démarrer. De quoi faire face à une concurrence féroce sur le marché des vaccins, alors que le recours à une troisième dose prend de l’ampleur en Europe. Les vaccins de Sanofi ou de Novavax, sur des technologies différentes, avancent aussi de leur côté et Pfizer/BioNTech continuent de dominer le secteur.
Au-delà de l’efficacité brute, un autre défi attend Valneva : celui de pouvoir produire son vaccin en quantité suffisante. Avec un site écossais qui a démarré sa production commerciale dès le début de l’année 2021, la biotech a des arguments à faire valoir. Elle devra cependant pouvoir fournir des garanties suffisantes pour espérer décrocher une commande d’ampleur, par exemple de l’Union européenne. Et poursuivre sa remontée.
En Bourse, le cours de la biotech s’est envolé de plus de 60 % dans les jours qui ont suivi l’annonce de ses résultats.